Enfermedad, metabolismo anaerobio y acidez tisular.

El ser humano es un organismo que necesita imperiosamente del oxígeno para vivir.
Aunque metabólicamente nuestras células se encuentran equipadas con la batería
enzimática capaz de generar energía en forma anaeróbica, este proceso es muy poco
eficiente y genera subproductos que conducen a la disfunción celular, tisular y
finalmente del organismo entero. Para poder aprovisionarse de oxígeno la naturaleza ha
dotado al hombre de un sistema respiratorio capaz de tomar el oxígeno del aire que lo
rodea, a la vez que le permite desechar subproductos que no necesita. Existe una
cuestión más, que también es una función del sistema respiratorio y es el rol que juega
en el mantenimiento de nuestro medio interno.
Asegurada la disponibilidad de O2 la naturaleza ha desarrollado un sistema altamente
eficiente de transporte, que le permite al organismo proveer de oxígeno a todas y cada
una de sus células, el sistema cardiovascular. Como todo, el sistema cardiovascular está
formado por varios componentes que, a grandes rasgos, son: una red cerrada de
conducción (arterias, arteriolas, capilares, vénulas y venas), una bomba (corazón) y un
tejido especializado que es la sangre. La sangre cumple varias funciones, los glóbulos
rojos son los vinculados al transporte de oxígeno. Dentro de los glóbulos rojos se
encuentra la proteína clave de todo el proceso, la hemoglobina, sin la cual fracasaría
toda la mecánica antes descripta.
El proceso de captura y liberación de oxígeno por parte de la hemoglobina varía en
función de varios factores, siendo los efectores fisiológicos más importantes: el pH
(grado de acidez o alcalinidad), la temperatura, la pCO2 (presión parcial de dióxido de
carbono, una medida del contenido de CO2), la pO2 (presión parcial de oxígeno) y el
2,3-difosfoglicerato (2,3-DPG). Para poder entender cómo estos efectores inciden en la
capacidad de la hemoglobina en tomar y ceder oxígeno debemos tener presente la curva
de disociación de la oxihemoglobina (HbO2):
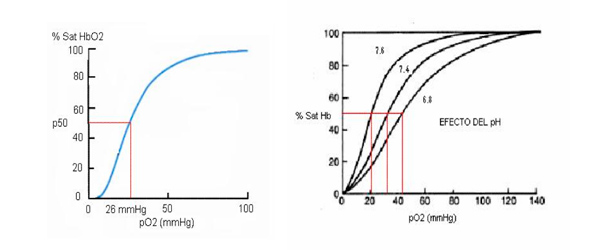
En el pulmón, la pO2 del aire alveolar es de alrededor de 100 mmHg, mientras que en el
músculo activo la pO2 es de alrededor de 20 mmHg. Puede apreciarse que en el pulmón
la hemoglobina toma O2 para quedar casi completamente saturada mientras que en los
tejidos ocurre lo opuesto: la hemoglobina libera el O2 para que sea tomado por las
células. Este proceso de liberación de oxígeno hacia los tejidos se encuentra favorecido
por la disminución del pH, el aumento de la temperatura, el aumento de la pCO2 y el
aumento del 2,3-DPG (desplazamiento de la curva de disociación de la HbO2 hacia la
derecha), todos estos efectores actúan por ejemplo en el músculo activo para mejorar el
aporte de oxígeno al tejido.
Sin embargo, todo esto es cierto cuando nos encontramos en condiciones fisiológicas.
Cuando a un tejido no le llega oxígeno (por ejemplo, debido a una isquemia) modifica
su metabolismo para adaptarse de las condiciones aeróbicas a las nuevas condiciones
anaeróbicas, entrando en un metabolismo fermentativo que, como dijimos al principio,
es muy poco eficiente (genera poco ATP). Cuando esto ocurre existe una
sobreproducción metabólica de ácidos produciendo un descenso del pH y una acidosis
tisular, siendo el lactato el principal subproducto. Si esto ocurre de un modo transitorio
y corto, los efectos de la acumulación de ácidos no producen mayores efectos sobre las
células (máxime si se producen en tejidos especialmente diseñados para soportarlo,
como el músculo). No obstante, cuando esta situación se extiende en el tiempo se
produce una alteración tanto funcional como morfológica de las células las que
conducirán finalmente a la desorganización del tejido, pérdida de la funcionalidad y
finalmente a la necrosis del mismo. Es conocido también el síndrome de isquemia-
reperfusión: un tejido que entró en metabolismo anaeróbico durante un tiempo
prolongado desarrolla una alteración funcional de tal magnitud que cuando mejora la
disponibilidad de oxígeno se vuelve incapaz de utilizarlo, debido quizás a una
disfunción mitocondrial, continúa en metabolismo anaerobio y desarrolla un gravísimo
estrés oxidativo. Finalmente, cuando ya se desarrolla una acidemia la hemoglobina
tomará menos oxígeno en los pulmones, por lo que llevará menos oxígeno a los tejidos,
generando consecuentemente más acidosis y así se desarrollará un círculo vicioso sin
fin. Del mismo modo, en los tejidos acidóticos también ocurre un mecanismo similar
puesto que aunque la Hb libera más O2 lo hace en las zonas iniciales que irriga el capilar
dejando al resto del tejido con menor disponibilidad de O2.
Si tenemos en cuenta nuestro medio interno, las células del organismo están
especialmente diseñadas para ser funcionales a un pH de 7,4 (alcalino) admitiendo solo
variaciones muy estrechas de ese valor. Resumiendo, nuestras células funcionan a pHs
alcalinos débiles, presentan una capacidad muy restringida para adaptarse a pHs ácidos
débiles y sólo pueden hacerlo durante un breve período de tiempo. Además, al ser
organismos estrictamente aerobios, nuestras células pueden aceptar no recibir oxígeno
por un breve período de tiempo. Pasado ese período, los productos generados por la
deficiente oxidación de los sustratos se vuelven tóxicos para la célula y conducen a su
disfunción y necrosis. Por tanto, podemos postular que la enfermedad podría tener su
origen en una primera agresión ácida a un tejido.
Un ejemplo que queremos analizar es el cáncer. En la actualidad se sostienen varias
teorías sobre la etiopatogenia de distintos tipos de cánceres y algunas otras sobre la
génesis de los mismos desde su origen primigenio. No obstante, son más las dudas que
las certezas que se tienen sobre el verdadero origen del cáncer.
Mucho se conoce sobre las características anatomopatológicas del cáncer pero
relativamente poco de su fisiología. Es sabido que las células tumorales poseen una muy
buena adaptabilidad metabólica, aunque no dejan de ser extremadamente dependientes
del aporte de oxígeno (obsérvese la neovascularización y la liberación de factores
angiogénicos por parte de las células tumorales), pero no se sabe cuáles son los factores
responsables de esta capacidad. Los tumores se inician con la reproducción desmedida
de las células neoplásicas, al principio sinmodificar mucho las características del medio
que las rodea. A medida que el tumor madura, en muchos casos, generan disminución
del pH de la zona, volviéndose ácidos. Un informe publicado en el “Cancer Research”
en el año 2005, postula que un factor que desencadena las metástasis es la hipoxia del
tumor y en el año 2009 se publica en la misma revista un informe que postula la
relación existente entre la acidez generada en el tumor con la capacidad invasiva y la
probabilidad de metástasis de las células neoplásicas.
Por lo antedicho, podemos teorizar sobre cuáles podrían ser las ventajas de utilizar una
droga alcalinizante utilizando como vehículo la mezcla O2/O3.
Veamos, si logramos alcalinizar la zona de desarrollo tumoral y llevarla a pH 7,4
podríamos mejorar la fisiología de las células normales de los alrededores del tejido
neoplásico y alterar el desarrollo del tumor al modificar el medio óptimo para su
crecimiento (medio ácido).
El aporte de la mezcla O2/O3 mejoraría el funcionamiento de las células normales, a la
vez que podría jugar un rol negativo sobre la célula cancerosa al modificar las vías
metabólicas que utiliza para su desarrollo óptimo (en general, los tumores producen un
desacople entre glucólisis y fosforilación oxidativa, utilizando la glucólisis como vía de
producción de intermediarios biosintéticos y la fosforilación oxidativa como fuente de
ATP). Además, las células neoplásicas podrían ser más propensas a los efectos que las
especies reactivas de oxígeno tienen sobre el material genético puesto que las células
tumorales están en fase de crecimiento rápido y su maquinaria de reparación del ADN
no funciona de un modo correcto (tienen una alta tasa de incidencia de nuevas
mutaciones).
Un detalle no menor es,que al utilizar como vehículoun gas podemos estar seguros que
el efecto que provoquemos será sobre todo el tejido y ocurrirá rápidamente. En caso de
que fuera una aplicación líquida tardaría mucho más ya que su velocidad de difusión es
muchísimo más lenta y a la vezpodría resultar enunefecto local únicamente.
Resumiendo, postulamos que una terapia local alcalinizante utilizando como vehículo
gas O2/O3 podría:
∙ Subir el pH a los rangos fisiológicos normales, mejorando el metabolismo de las
células normales.
∙ Al cambiar el medio de desarrollo de las células neoplásicas, provocaríamos una
acción deletérea sobre su crecimiento y metabolismo.
∙ Mejoraríamos la capacidad de nuestras células del sistema inmunitario para que
actúensobre el tumor
∙ Con la mezcla O2/O3 activaríamos el metabolismo de las células normales y
afectaríamos negativamente el desarrollo tumoral debido a su mayor
vulnerabilidad a los efectos de las especies reactivas del oxígeno.
Dr. Francisco Bacchetta
Químico

 Asociación Argentina del Ozono - ADELO
Asociación Argentina del Ozono - ADELO